Введение
Острый разрыв ахиллова сухожилия - одно из наиболее частых повреждений сухожилий нижней конечности, частота которого неуклонно растёт в последние десятилетия. Типичный пациент - мужчина 30-50 лет, занимающийся рекреационным спортом (так называемые weekend warriors). Разрыв происходит в зоне относительной гиповаскулярности (watershed zone) на 2-6 см проксимальнее прикрепления к пяточной кости - той же области, где развивается midportion-тендинопатия.
Выбор метода лечения - оперативного или консервативного - остаётся одним из наиболее дискутируемых вопросов в ортопедии. Современные данные свидетельствуют, что при использовании протоколов функциональной реабилитации с ранней нагрузкой и контролируемым движением результаты консервативного лечения приближаются к оперативным. Однако для ряда пациентов - прежде всего молодых спортсменов и лиц с большим диастазом между культями - хирургическое лечение по-прежнему обеспечивает лучшие функциональные результаты и более быстрый возврат к активности.
Ахиллово сухожилие несёт колоссальные нагрузки: до 6-8 массы тела при ходьбе и до 12.5 массы тела при беге. Утрата его целостности приводит к выраженному нарушению функции стопы и голеностопного сустава, невозможности бега, прыжков и подъёма на носок. Без адекватного лечения пациенты нередко испытывают стойкий функциональный дефицит, влияющий на качество повседневной жизни и трудоспособность.
В настоящем обзоре обобщены данные монографии Adams (2023) и актуальных рандомизированных исследований.
Эпидемиология
Заболеваемость острым разрывом ахиллова сухожилия увеличивается во всём мире на протяжении последних нескольких десятилетий. По данным популяционных исследований из Скандинавии, частота составляет 18-37 случаев на 100 000 населения в год с тенденцией к росту.
Пик приходится на возраст 30-50 лет. Соотношение мужчин и женщин составляет примерно 5-6:1. Левая (недоминантная) нога повреждается несколько чаще, что связано с её функцией толчковой конечности при отталкивании.
Второй, меньший пик заболеваемости наблюдается у пациентов старше 60 лет с дегенеративными изменениями сухожилия и сопутствующими медикаментозными факторами риска.
Факторы риска:
- Приём фторхинолонов (офлоксацин, ципрофлоксацин) - повышают риск разрыва в 3-4 раза, особенно у пациентов старше 60 лет и при одновременном приёме кортикостероидов
- Локальные инъекции кортикостероидов в область сухожилия или паратенона
- Системная терапия глюкокортикостероидами
- Сахарный диабет (микроангиопатия ухудшает кровоснабжение сухожилия)
- Хроническая болезнь почек
- Ревматоидный артрит и другие системные воспалительные заболевания
- Ожирение (повышенная механическая нагрузка на сухожилие)
Наиболее часто разрыв ахиллова сухожилия происходит при занятиях баскетболом, футболом, теннисом и бегом - видами спорта, характеризующимися резким ускорением и торможением, прыжками и внезапной сменой направления движения. Характерно, что разрыв чаще происходит у рекреационных атлетов, нежели у профессионалов, что объясняется нерегулярным режимом тренировок и недостаточной физической подготовкой.
Этиология и механизм
Ахиллово сухожилие формируется слиянием апоневрозов трёх головок трёхглавой мышцы голени: медиальной и латеральной головок икроножной мышцы (m. gastrocnemius) и камбаловидной мышцы (m. soleus). Это самое крупное и прочное сухожилие человеческого тела длиной 12-15 см, прикрепляющееся к задней поверхности пяточного бугра. Сухожилие окружено паратеноном (а не синовиальным влагалищем), который обеспечивает скольжение и васкуляризацию.
Основные механизмы разрыва:
- Резкое мощное подошвенное сгибание против сопротивления (отталкивание, прыжок) - наиболее частый механизм
- Эксцентрическая перегрузка при тыльном сгибании стопы (приземление после прыжка)
- Внезапное тыльное сгибание при расслабленной стопе (оступание, падение в яму, соскальзывание со ступеньки)
- Прямая травма (удар по натянутому сухожилию) - встречается редко
Зона разрыва в подавляющем большинстве случаев располагается на 2-6 см проксимальнее прикрепления к пяточному бугру. Эта зона совпадает с watershed zone - участком относительной гиповаскулярности сухожилия, где кровоснабжение минимально. Именно в этой зоне сходятся сосуды, питающие сухожилие проксимально (из мышечно-сухожильного перехода) и дистально (из костного прикрепления), формируя область наименьшей перфузии.
Дегенеративные изменения (предшествующая тендинопатия, мукоидная дегенерация, гиперваскулярность, липоматозная инфильтрация) часто обнаруживаются гистологически в зоне разрыва. Это указывает на хроническую предсуществующую патологию, предрасполагающую к разрыву. Истинно здоровое сухожилие рвётся крайне редко - в большинстве случаев разрыв происходит на фоне субклинической дегенерации.
Ахиллово сухожилие в норме способно выдерживать нагрузки до 12.5 массы тела при беге. Разрыв происходит, когда механическая нагрузка превышает прочность дегенеративно изменённого сухожилия. Многие пациенты ретроспективно вспоминают эпизоды дискомфорта или боли в области сухожилия за недели и месяцы до разрыва.
Клиническая картина и диагностика
Типичная картина: внезапный щелчок или ощущение удара по задней поверхности голени во время физической активности. Пациент описывает ощущение как pop или kick in the back of the ankle. Нередко пациент оборачивается, ожидая увидеть ударившего его человека. Боль может быть удивительно умеренной для столь серьёзной травмы - это объясняется разрывом дегенеративно изменённой, частично денервированной ткани.
В первые 24-48 часов пальпируется западение (gap) в проекции сухожилия; позже отёк и гематома маскируют дефект, затрудняя клиническую диагностику. Пациент не может встать на носок на поражённой ноге, хотя активное подошвенное сгибание против гравитации может частично сохраняться.
Сохранение активного подошвенного сгибания за счёт длинного сгибателя пальцев (m. flexor digitorum longus), задней большеберцовой мышцы (m. tibialis posterior) и малоберцовых мышц (mm. peronei) создаёт ложное впечатление интактности сухожилия. Это приводит к пропуску диагноза в 20-25% случаев при первичном обращении. Задержка диагностики существенно ухудшает результаты лечения, поскольку ретракция культей и рубцевание снижают возможности как консервативного, так и хирургического лечения.
Клинические тесты
Тест Томпсона (Simmonds) - наиболее надёжный одиночный тест. Пациент лежит на животе, стопа свободно свисает за край кушетки. Врач двумя руками сжимает икроножную мышцу в средней трети. В норме стопа совершает пассивное подошвенное сгибание за счёт передачи усилия через интактное сухожилие. При разрыве сухожилия подошвенное сгибание отсутствует или значительно ослаблено (положительный тест). Чувствительность теста составляет 96-100%. Важно сравнивать со здоровой стороной.
Тест Мэтлза (Matles). Пациент на животе, оба колена согнуты под 90 градусов в расслабленном состоянии. На стороне разрыва стопа свисает в нейтральном положении или тыльном сгибании, тогда как здоровая стопа остаётся в положении подошвенного сгибания (10-15 градусов). Тест оценивает тонус мышечно-сухожильной единицы трёхглавой мышцы голени в покое и прост в выполнении.
Игольчатый тест О’Брайена (O’Brien needle test). Игла 25G вводится через кожу в сухожилие на 10 см проксимальнее инсерции. При пассивном тыльном сгибании стопы игла в норме отклоняется за счёт натяжения интактного сухожилия. Если игла остаётся неподвижной - сухожилие разорвано дистальнее точки введения. Тест особенно полезен при отёчных тканях, когда пальпация дефекта затруднена.
Тест Копланда (Copeland). Манжета сфигмоманометра накладывается на голень и накачивается до 100 мм рт.ст. При пассивном тыльном сгибании стопы давление в норме возрастает до 140+ мм рт.ст. за счёт увеличения объёма голени при натяжении интактного сухожилия. Отсутствие повышения давления указывает на разрыв.
Для повышения диагностической точности рекомендуется использовать комбинацию нескольких тестов. Сочетание теста Томпсона, теста Мэтлза и пальпации дефекта обеспечивает чувствительность, близкую к 100%.
Инструментальная диагностика
Ультразвуковое исследование (УЗИ) - метод первого выбора при подозрении на разрыв ахиллова сухожилия. Чувствительность 92-100%, специфичность 83-100%. Основные преимущества: доступность, отсутствие лучевой нагрузки, низкая стоимость, возможность динамической оценки в режиме реального времени.
Динамическая оценка: при тыльном сгибании визуализируется диастаз между культями; при подошвенном сгибании оценивается аппозиция концов. Измерение остаточного диастаза при максимальном подошвенном сгибании имеет ключевое прогностическое значение для выбора тактики лечения (порог 5-10 мм).
При УЗИ оценивают:
- Наличие и локализацию разрыва (полный или частичный)
- Размер диастаза в нейтральном положении и при максимальном подошвенном сгибании
- Качество проксимальной и дистальной культей (степень дегенерации, разволокнение)
- Наличие интерпозиции гематомы или жировой ткани между культями
- Состояние паратенона
- Наличие жидкости в пери- и паратендинозном пространстве
МРТ показана в сомнительных случаях, при подозрении на частичный разрыв, при хронических разрывах или для предоперационного планирования. При остром полном разрыве МРТ не является обязательным исследованием, если клинический диагноз и данные УЗИ однозначны. МРТ информативна для оценки дегенеративных изменений в оставшейся ткани сухожилия и исключения сопутствующей патологии (костный отёк пяточной кости, тендинопатия других сухожилий).
Дифференциальная диагностика
При клиническом подозрении на разрыв ахиллова сухожилия необходимо исключить:
- Разрыв подошвенной мышцы (m. plantaris) - так называемый tennis leg: острая боль в икроножной области, но тест Томпсона отрицательный, подъём на носок сохранён
- Разрыв медиальной головки икроножной мышцы - гематома и отёк в средней трети голени, тест Томпсона отрицательный
- Тромбоз глубоких вен голени - постепенное начало, диффузный отёк, болезненность при пальпации глубоких вен
- Отрывной перелом пяточного бугра - боль в области прикрепления, рентгенография подтверждает диагноз
- Задний импинджмент голеностопного сустава - хроническая боль при подошвенном сгибании, тест Томпсона отрицательный
- Частичный разрыв ахиллова сухожилия - сохранена непрерывность, но снижена прочность; УЗИ или МРТ для уточнения
Лечение
Выбор между оперативным и консервативным лечением остаётся дискуссионным. Традиционная точка зрения отдавала предпочтение хирургическому лечению из-за меньшей частоты повторных разрывов. Современные данные демонстрируют, что при использовании протоколов функциональной реабилитации с ранней нагрузкой и ранним контролируемым движением консервативное лечение обеспечивает сопоставимые функциональные результаты, но с более высокой частотой повторных разрывов (4-12% vs 2-5%). [Hanselman, 2023; Willits et al., 2010]
Ключевые факторы при принятии решения:
- Уровень физической активности и спортивные требования пациента
- Размер диастаза между культями при динамическом УЗИ (порог 5-10 мм)
- Возраст и соматический статус (курение, диабет, заболевания сосудов)
- Сроки от момента травмы (острый разрыв - до 3 недель, подострый - 3-6 недель, хронический - более 6 недель)
- Предпочтения пациента после информированного обсуждения рисков и преимуществ
Консервативное лечение
Эволюция подхода: от длительной иммобилизации гипсовой повязкой (8 недель, частота повторного разрыва 12-36%) к современным протоколам функциональной реабилитации с существенно лучшими результатами. Устаревшие протоколы длительной иммобилизации без нагрузки ассоциируются с неприемлемо высокой частотой повторных разрывов и не должны применяться. [Glazebrook, 2023]
Ключевые принципы современного консервативного лечения:
- Ранняя осевая нагрузка (с 2-й недели)
- Раннее контролируемое движение (ECM - early controlled motion, с 3-й недели)
- Динамическое УЗИ-мониторирование диастаза на 2-й и 6-й неделе
- Функциональный ортез (walking boot) вместо циркулярного гипса
Прогностический фактор: размер диастаза между культями при максимальном подошвенном сгибании (динамическое УЗИ). Порог - 5-10 мм. Пациенты с диастазом более 10 мм имеют худшие функциональные результаты (более низкие значения ATRS) и более высокую частоту повторных разрывов. Для этой группы пациентов следует рассмотреть переход к оперативному лечению. [Barfod et al., 2019]
Протокол функциональной реабилитации:
- 0-2 недели: гипсовая лонгета или ортез в положении подошвенного сгибания (эквинус 20-30 градусов), без нагрузки или частичная нагрузка на пятку. Контрольное УЗИ на 2-й неделе
- 2-4 недели: ходьба в ортезе (walking boot) с подпяточными клиньями (3 клина, общая высота 3-4 см), полная осевая нагрузка
- 4-6 недель: прогрессивное удаление клиньев (по одному каждые 2 недели), начало активных упражнений на амплитуду движений. Контрольное УЗИ на 6-й неделе
- 6-8 недель: ортез без клиньев, активное тыльное сгибание до нейтрального положения, укрепляющие упражнения
- 8 недель: снятие ортеза, переход к полноценной программе реабилитации
Результаты: частота повторного разрыва при функциональной реабилитации составляет 4-12% (по сравнению с 2-5% при оперативном лечении). По данным РКИ Willits et al. (2010), функциональные результаты (Leppilahti score) не различались между группами оперативного и консервативного лечения при сроке наблюдения 2 года. [Costa et al., 2020; Willits et al., 2010]
Ранняя нагрузка улучшает функциональные показатели (SMFA, ATRS), ускоряет возврат к ходьбе без увеличения риска повторного разрыва. Okoroha et al. (2020) показали, что пациенты с ранней нагрузкой возвращались к полноценной ходьбе без ортеза на 3 недели раньше контрольной группы.
Раннее контролируемое движение снижает частоту повторного разрыва, ускоряет возврат к работе и улучшает ATRS по сравнению со строгой иммобилизацией. [Brumann et al., 2014]
Частота тромбоза глубоких вен при консервативном лечении достигает 47.7%, что является значимой клинической проблемой. Необходимо информировать пациента о симптомах тромбоза. Химиопрофилактика тромбоза (низкомолекулярные гепарины) рекомендуется в период иммобилизации. Ранняя нагрузка и движение частично снижают этот риск.
Хирургическое лечение
Миниинвазивная техника (PARS-Dresden)
Перкутанная система восстановления ахиллова сухожилия (Percutaneous Achilles Repair System, PARS) в дрезденской модификации представляет собой миниинвазивную методику, сочетающую преимущества открытого шва (прочная фиксация, визуальный контроль зоны разрыва) с минимальной хирургической травмой мягких тканей.
Показания: молодые активные пациенты в сроки до 3 недель после травмы, при адекватном качестве тканей дистальной культи.
Противопоказания: неамбулаторные пациенты; тяжёлые декомпенсированные соматические заболевания; курение и сахарный диабет (относительные); хронический разрыв с выраженной ретракцией и дегенерацией культей.
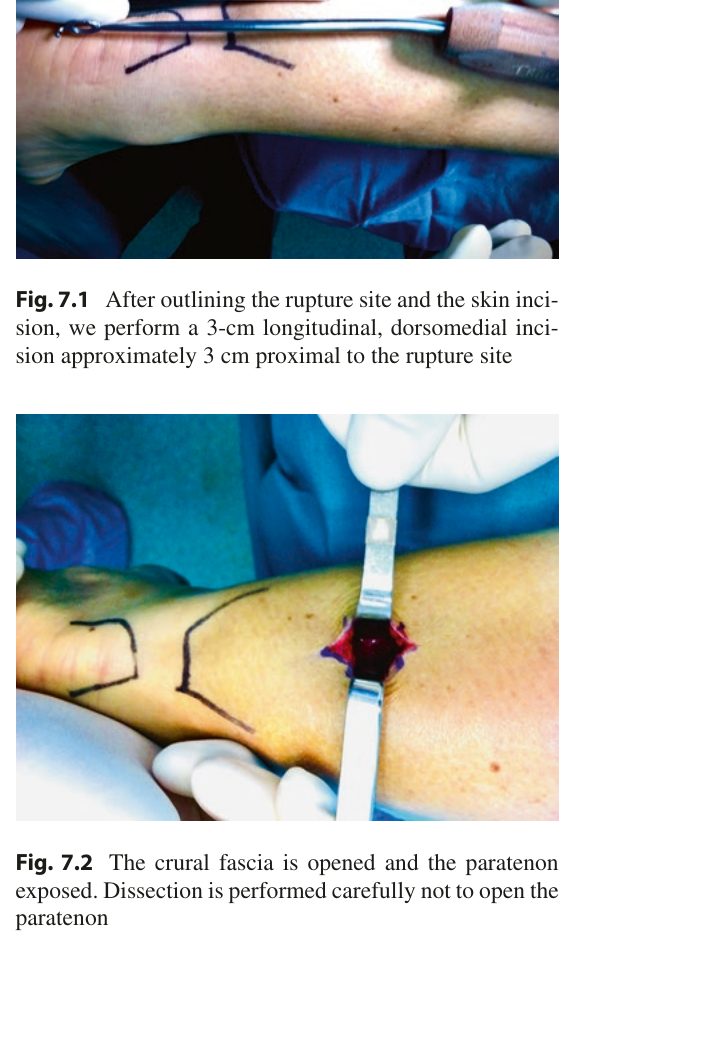
Рис. 1. Миниинвазивная техника PARS-Dresden: (сверху) определение зоны разрыва, разметка разреза - 3 см продольный разрез в 1 см от зоны разрыва; (снизу) фасция голени открыта, паратенон обнажён. Адаптировано из Adams, 2023
Техника: пациент в положении на животе под региональной или общей анестезией. Зона разрыва определяется пальпаторно и подтверждается УЗИ. Выполняется продольный разрез длиной 3 см латерально, в 1 см от пальпируемого дефекта. Фасция голени рассекается продольно, обнажается паратенон.
Дрезденские инструменты (специализированные направители с каналами для нитей) вводятся субфасциально, между фасцией голени и паратеноном - медиально и латерально от сухожилия. Принципиально важно, что инструменты проходят между фасцией и паратеноном, а не субкутанно - это снижает риск повреждения икроножного нерва.
Две нити FiberWire 2.0 проводятся через дистальную культю в X-образной конфигурации пилящим движением (see-saw motion). Инструменты извлекаются через проксимальный мини-разрез (2 см) с аксиальной тракцией. Нити затягиваются в положении максимального подошвенного сгибания стопы. Тест Мэтлза выполняется интраоперационно для контроля адекватности натяжения - положение стопы должно быть симметрично контралатеральной стороне.
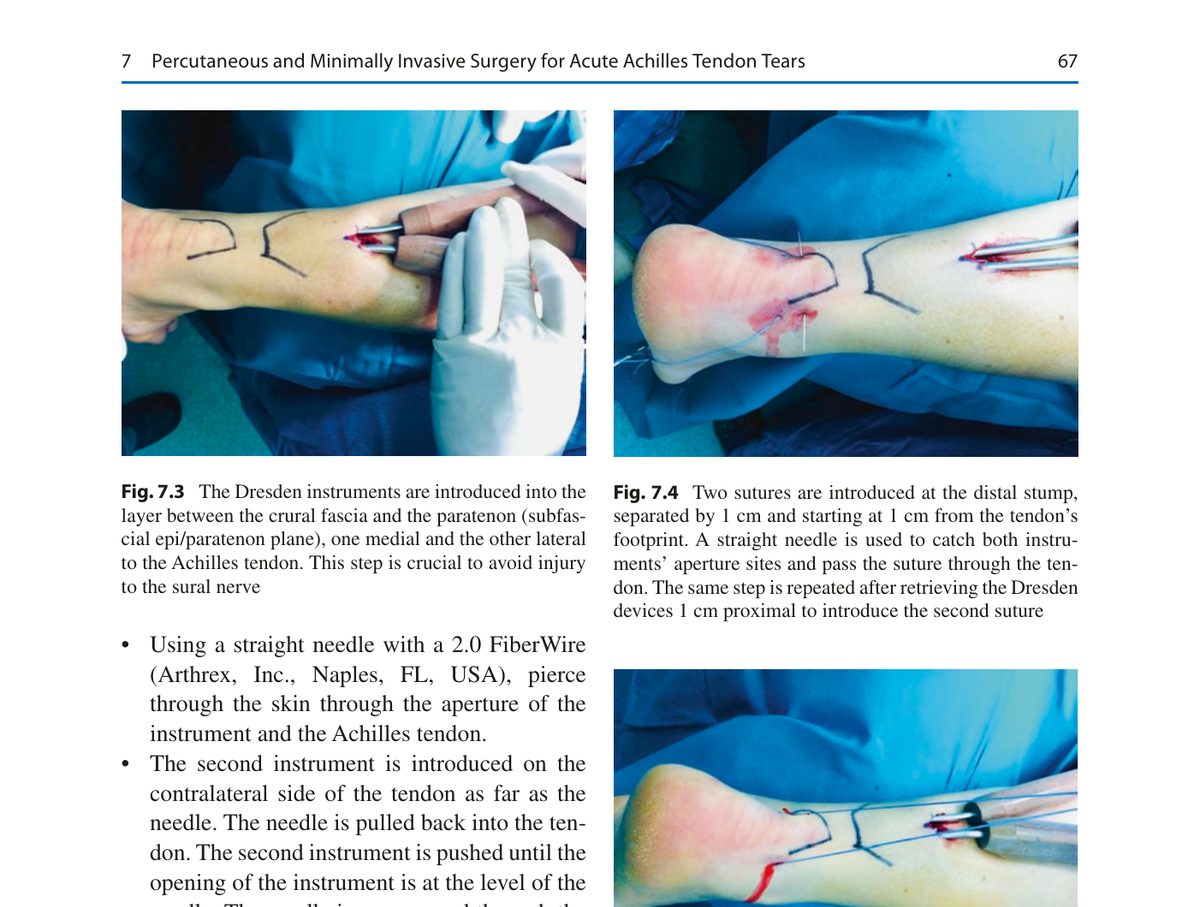
Рис. 2. Техника PARS-Dresden: (a) дрезденские инструменты введены между фасцией голени и паратеноном, медиально и латерально от сухожилия; (b) две нити FiberWire проведены через дистальную культю; (c) инструмент извлечён через проксимальный разрез с аксиальной тракцией. Адаптировано из Adams, 2023
Преимущества методики:
- Сохранение кровоснабжения (паратенон интактен, перитендинозные сосуды не повреждены)
- Малый разрез (3 см основной + 2 см проксимальный) и меньшая частота раневых осложнений
- Функциональные результаты (ATRS) сопоставимы с открытым швом
- Более ранний возврат к работе по сравнению с открытым доступом
- Лучший косметический результат
- Меньшая послеоперационная боль
Риск повреждения икроножного нерва минимизирован за счёт латерального доступа и проксимального направления проведения инструментов. Субфасциальное (а не субкутанное) проведение инструментов дополнительно снижает вероятность контакта с нервом, который проходит субкутанно.
Результаты: частота повторного разрыва менее 3%, расхождение раны менее 4%. По данным Metz et al. (2008), миниинвазивный шов обеспечивал более быстрый возврат к работе по сравнению с консервативным лечением при сопоставимых функциональных результатах. [Espinoza et al., 2023; Metz et al., 2008]
Открытый шов
Показания: острый разрыв (особенно при большом диастазе и невозможности адекватной аппозиции миниинвазивно), неудача консервативного лечения, спортсмены, стремящиеся к максимальной надёжности восстановления, невозможность выполнения миниинвазивного шва (хронический разрыв более 3-6 недель, выраженная ретракция культей).
Доступ: продольный заднемедиальный разрез длиной 8-12 см по медиальному краю сухожилия. Медиальный доступ позволяет избежать повреждения икроножного нерва (n. suralis), расположенного латерально. Рассекают кожу, подкожную клетчатку, паратенон. Паратенон по возможности сохраняют и ушивают в конце операции отдельным слоем для оптимизации скольжения сухожилия и заживления.
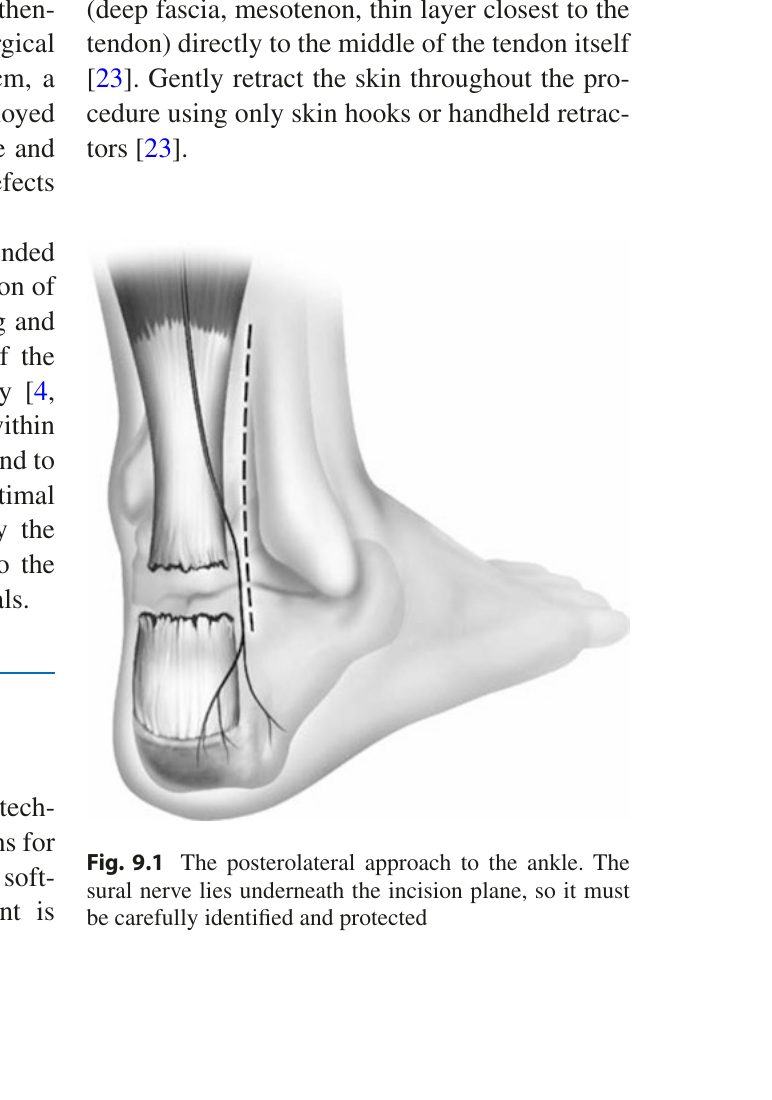
Рис. 3. Открытый доступ к ахиллову сухожилию: продольный заднемедиальный разрез. Адаптировано из Adams, 2023
Техника: идентификация и ревизия концов сухожилия, дебридмент размягчённых и дегенеративно изменённых тканей при необходимости. Гематому эвакуируют. Оценивают качество проксимальной и дистальной культей, а также возможность адекватной адаптации без избыточного натяжения.
Основной шов (core suture) выполняется одной из стандартных техник:
- Шов по Кракову (Krackow) - замыкающий шов с петлями, обеспечивающий равномерное распределение нагрузки
- Шов по Tajima - замыкающий шов с крестообразной конфигурацией
- Шов по Баннеллу (Bunnell) - зигзагообразный шов через толщу сухожилия
Дополнительно накладывается обвивной эпитендинозный шов (running epitendinous suture) для улучшения аппозиции поверхности, снижения зазоров между культями и увеличения общей прочности конструкции.
Модифицированный шов по Tajima - четырёхниточная (4-strand) техника с замыкающими петлями. Биомеханически четырёхниточный шов значительно прочнее двухниточного (примерно в 1.5-2 раза по нагрузке на разрыв), что обеспечивает возможность более ранней мобилизации и снижает риск повторного разрыва в раннем послеоперационном периоде. [Moorman, Kaseta, 2023]

Рис. 4. Шов по Tajima: четырёхниточная модификация для открытого шва ахиллова сухожилия. Адаптировано из Adams, 2023
При большом диастазе или дефекте тканей, когда прямая адаптация концов невозможна без избыточного натяжения, применяются варианты аугментации:
- Turndown-лоскут из проксимальной культи (V-Y пластика или ротационный лоскут из центральной порции проксимального отрезка)
- Сухожилие подошвенной мышцы (plantaris) в качестве биологического каркаса, обернутого вокруг зоны шва
- Транспозиция сухожилия длинного сгибателя большого пальца (FHL transfer) - наиболее надёжный метод аугментации при дефектах более 3 см; FHL проходит анатомически рядом с ахилловым сухожилием и обеспечивает дополнительную силу подошвенного сгибания
Осложнения открытого шва:
- Расхождение раны: 3-8% (наиболее частое хирургическое осложнение)
- Инфекция (поверхностная и глубокая): 2-4%
- Повреждение икроножного нерва: 3-5% (проявляется парестезией по наружному краю стопы)
- Тромбоз глубоких вен
- Повторный разрыв: 2-5%
- Формирование гипертрофического рубца и спаечный процесс
- Нарушение кожной чувствительности в области рубца
Лечение у спортсменов
Большинство профессиональных спортсменов предпочитают оперативное лечение, поскольку оно обеспечивает более быстрый возврат к спорту: 6-9 месяцев при оперативном лечении по сравнению с 9-12 месяцами при консервативном. Оперативное лечение также даёт спортсмену психологическую уверенность в прочности восстановленного сухожилия. [Madi et al., 2023]
К преинжурному уровню спортивной активности возвращаются лишь 60-80% пациентов. Дефицит силы подошвенного сгибания в 10-15% сохраняется даже после полного восстановления и является одной из причин неполного возврата к спорту. У спринтеров и прыгунов этот дефицит наиболее критичен; у игроков командных видов спорта - менее значим.
Факторы, влияющие на возврат к спорту:
- Возраст на момент травмы (моложе - лучше прогноз)
- Уровень спортивной активности до травмы
- Метод лечения и качество реабилитации
- Психологическая готовность (страх повторной травмы - частая причина неполного возврата)
- Вид спорта (контактные vs неконтактные, прыжковые vs циклические)
Реабилитация
Протоколы реабилитации после оперативного и консервативного лечения во многом схожи. Ключевой принцип - прогрессивное увеличение нагрузки при контролируемой защите зоны шва или регенерата. Биологическое созревание сухожильной ткани занимает 6-12 месяцев, и программа реабилитации должна учитывать этот временной фактор. Слишком агрессивная ранняя нагрузка опасна повторным разрывом; слишком консервативный подход - потерей подвижности и атрофией мышц. [Allahabadi et al., 2023]
Этапы реабилитации
Фаза 1 (0-2 недели): защита и контроль отёка. Иммобилизация в положении эквинуса (подошвенное сгибание 20-30 градусов). При оперативном лечении - без нагрузки или минимальная нагрузка на пятку. При консервативном - допускается ранняя осевая нагрузка в ортезе. Криотерапия, возвышенное положение конечности, изометрические упражнения для четырёхглавой мышцы и мышц тазобедренного сустава.
Фаза 2 (2-6 недель): ранняя мобилизация. Ходьба в ортезе (walking boot) с подпяточными клиньями. Прогрессивная осевая нагрузка до полной. Осторожные упражнения на амплитуду движений: активное подошвенное сгибание, пассивное тыльное сгибание до нейтрали (не дальше). Последовательное удаление клиньев (по одному каждые 2 недели). Упражнения в бассейне при зажившей ране (ходьба в воде, движения стопой).
Важно: в фазе 2 категорически запрещается пассивное тыльное сгибание за нейтральное положение, растяжка икроножной мышцы и любые упражнения с эксцентрическим компонентом. Эти ограничения направлены на предотвращение удлинения зоны регенерата.
Фаза 3 (6-12 недель): восстановление движений и начало укрепления. Снятие ортеза. Активные упражнения на восстановление полной амплитуды тыльного и подошвенного сгибания. Переход от изометрических упражнений к концентрическим и затем эксцентрическим (протокол Alfredson с модификациями). Нормализация паттерна походки. Велоэргометр с низким сопротивлением. Подъём на двух ногах на носки (bilateral heel raise).
Критерии перехода от фазы 3 к фазе 4: полная амплитуда тыльного сгибания (симметрично здоровой стороне), безболезненный подъём на носки на двух ногах не менее 15 повторений, нормализованный паттерн ходьбы без хромоты.
Фаза 4 (3-6 месяцев): прогрессивное укрепление. Силовые упражнения с сопротивлением: жим ногами, подъём на носок одной ногой с отягощением, приседания. Тренировка проприоцепции на нестабильных платформах (BOSU, балансборд). Коррекция асимметрии походки. Бег трусцой по прямой с 4-го месяца при достаточной силе (25 повторений подъёма на носок одной ногой без боли). Плавание и глубоководный бег.
Критерии перехода от фазы 4 к фазе 5: подъём на носок на одной ноге не менее 15 повторений без боли, бег трусцой 20 минут без боли и отёка, сила подошвенного сгибания не менее 70% от контралатеральной стороны (изокинетическое тестирование при возможности).
Фаза 5 (6-12 месяцев): возврат к спорту. Спорт-специфическая тренировка. Плиометрические упражнения (прыжки, скачки, бег с ускорением). Упражнения со сменой направления, боковые перемещения. Постепенное увеличение объёма и интенсивности тренировок. Тестирование готовности к возврату к полной спортивной нагрузке.
Критерии возврата к спорту
Возврат к полноценной спортивной активности допускается при выполнении совокупности критериев:
- Симметричный подъём на носок на одной ноге: не менее 80% от контралатеральной стороны по количеству повторений и высоте подъёма (в идеале не менее 25 повторений)
- ATRS (Achilles tendon Total Rupture Score) более 80 баллов из 100
- Положительный тест прыжка на одной ноге (single-leg hop test): не менее 80% от здоровой стороны по дистанции
- Успешное выполнение спорт-специфических тестов (ускорения, торможения, смена направления, прыжки)
- Отсутствие боли и отёка при нагрузках
- Психологическая готовность и уверенность спортсмена (отсутствие страха повторной травмы)
Для объективной оценки готовности рекомендуется использовать стандартизированные инструменты: опросник ATRS для субъективной оценки функции, изокинетическое тестирование для объективной оценки силы подошвенного сгибания, а также функциональные тесты (single-leg hop, side hop, countermovement jump) для оценки взрывной силы и нервно-мышечного контроля.
Возврат к тренировочному процессу рекомендуется выполнять поэтапно: сначала индивидуальные тренировки без контакта, затем командные тренировки с ограничениями, далее полноценные тренировки, и только после этого - соревновательная деятельность. Каждый этап должен занимать не менее 2-3 недель.
Индивидуальное тестирование должно проводиться спортивным врачом или реабилитологом. Решение о допуске к полноценным тренировкам принимается коллегиально с учётом объективных критериев и субъективной готовности спортсмена.
Преждевременный возврат к спорту (до 6 месяцев после травмы) ассоциируется с повышенным риском повторного разрыва и не рекомендуется.
Осложнения
Осложнения варьируются в зависимости от метода лечения.
При консервативном лечении:
- Повторный разрыв: 4-12% при функциональной реабилитации (основное опасение)
- Тромбоз глубоких вен: до 47.7% (наиболее частое серьёзное осложнение)
- Удлинение сухожилия (tendon elongation) и стойкое снижение силы подошвенного сгибания
- Длительная слабость трёхглавой мышцы голени, атрофия
- Ригидность голеностопного сустава при длительной иммобилизации
При оперативном лечении:
- Раневые осложнения (расхождение краёв раны, некроз краёв кожного лоскута, поверхностная инфекция): 3-8%
- Глубокая инфекция: 2-4%
- Повреждение икроножного нерва: 3-5% (проявляется онемением и парестезией по наружному краю стопы)
- Повторный разрыв: 2-5%
- Тромбоз глубоких вен
- Формирование гипертрофического или келоидного рубца, спаечный процесс
- Нарушение кожной чувствительности в области послеоперационного рубца
Миниинвазивные методики (PARS-Dresden) снижают частоту раневых осложнений и повреждения нерва при сопоставимой частоте повторного разрыва и функциональных результатах. По данным Metz et al. (2008) и Espinoza et al. (2023), миниинвазивный шов ассоциируется с более быстрым возвратом к работе и меньшей частотой осложнений раны.
Удлинение сухожилия (tendon elongation) - специфическое осложнение, характерное для консервативного лечения. Удлинение сухожилия на 5 мм и более приводит к клинически значимому снижению силы подошвенного сгибания и выносливости трёхглавой мышцы голени. Контроль длины сухожилия с помощью динамического УЗИ на 6-й и 12-й неделе позволяет своевременно выявить это осложнение.
Прогноз
Функциональные результаты лечения в целом благоприятны, однако полного восстановления достигают не все пациенты. Дефицит силы подошвенного сгибания в 10-15% сохраняется длительно вне зависимости от метода лечения. К преинжурному уровню спортивной активности возвращаются 60-80% пациентов; остальные вынуждены снижать уровень нагрузок или менять вид активности.
Факторы, ассоциированные с худшим прогнозом:
- Большой диастаз при динамическом УЗИ (более 10 мм при подошвенном сгибании)
- Возраст старше 50 лет
- Курение (нарушение микроциркуляции, замедление заживления)
- Ожирение (ИМТ более 30)
- Сахарный диабет
- Позднее начало лечения (хронический разрыв)
- Позднее начало реабилитации
- Несоблюдение протокола реабилитации
- Задержка диагностики (переход в хронический разрыв)
При хроническом разрыве (диагностированном позднее 6 недель от момента травмы) прогноз существенно хуже: ретракция культей, рубцевание и атрофия мышц затрудняют восстановление и часто требуют аугментационных методик (FHL transfer, V-Y пластика).
Отдалённые результаты (5-10 лет наблюдения) показывают, что большинство пациентов удовлетворены результатами лечения вне зависимости от выбранного метода. Различия в частоте повторных разрывов между оперативным и консервативным лечением нивелируются при использовании современных протоколов функциональной реабилитации. Ключевое значение имеет не столько метод лечения, сколько качество последующей реабилитации и приверженность пациента рекомендованному протоколу.
Ранняя функциональная реабилитация с контролируемой нагрузкой и движением улучшает результаты вне зависимости от выбранного метода лечения. Решение об оперативном или консервативном подходе должно приниматься индивидуально с учётом возраста, уровня активности, данных динамического УЗИ и предпочтений пациента после информированного обсуждения рисков и преимуществ каждого метода.
Источники
- Hanselman AE. Summary of Data Comparing Nonoperative, Open, and Minimally Invasive Treatment of Achilles Tendon Tears. In: Adams SB, ed. The Achilles Tendon. Springer; 2023:33-42.
- Glazebrook M. Nonoperative Treatment of Acute Achilles Tendon Rupture. In: Adams SB, ed. The Achilles Tendon. Springer; 2023:43-52.
- Espinoza RM et al. Percutaneous and Minimally Invasive Surgery for Acute Achilles Tendon Tears. In: Adams SB, ed. The Achilles Tendon. Springer; 2023:61-74.
- Moorman CT, Kaseta MK. Traditional Open Repair of Achilles Tendon Tears. In: Adams SB, ed. The Achilles Tendon. Springer; 2023:81-90.
- Madi NS et al. Management of Achilles Tendon Tears in Athletes. In: Adams SB, ed. The Achilles Tendon. Springer; 2023:91-100.
- Allahabadi S et al. Rehabilitation of Achilles Tendon Tears (Operative and Nonoperative). In: Adams SB, ed. The Achilles Tendon. Springer; 2023:111-125.
- Okoroha KR et al. Early vs delayed weight-bearing after Achilles tendon repair. J Bone Joint Surg. 2020;102:1720-1726.
- Costa ML et al. Plaster cast versus functional bracing for Achilles tendon rupture: the UKSTAR RCT. Health Technol Assess. 2020;24(8).
- Barfod KW et al. Nonoperative, dynamic treatment of acute Achilles tendon rupture. Knee Surg Sports Traumatol Arthrosc. 2019;27:3385-3393.
- Brumann M et al. Accelerated rehabilitation following Achilles tendon repair after acute rupture: a systematic review. BMC Musculoskelet Disord. 2014;15:100.
- Metz R et al. Acute Achilles tendon rupture: minimally invasive surgery versus nonoperative treatment with immediate full weightbearing. Am J Sports Med. 2008;36:1688-94.
- Willits K et al. Operative versus nonoperative treatment of acute Achilles tendon ruptures: a multicenter RCT. J Bone Joint Surg Am. 2010;92(17):2767-75.